Строительные работы в Севастополе
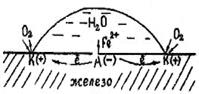
Под электрохимической коррозией подразумевают процесс взаимодействия металлов с электролитами в виде водных растворов, реже с неводными электролитами, например, с некоторыми органическими электропроводными соединениями или безводными расплавами солей при повышенных температурах. Делится на электрокоррозию и гальванокоррозию. Из указанных разновидностей рассмотрим лишь гальванокоррозию. 2.2.1 Электрохимическая гальванокоррозия. Электрохимическая коррозия – наиболее распространенный вид коррозии металлов. Примером коррозионных процессов электрохимического характера является разрушение деталей машин, приборов и различных металлических конструкций в почвенных, грунтовых, речных и морских водах, в атмосфере под адсорбированными пленками влаги, в технических растворах. Растворенный кислород и ионы водорода – важнейшие окислители, вызывающие электрохимическую коррозию металлов. Рассмотрим схему этого процесса. Сложность его заключается в том, что на одной и той же поверхности происходят одновременно два процесса, противоположные по своему химическому смыслу: окисление металла и восстановление окислителя. Оба процесса должны протекать сопряженно, чтобы сохранялось равенство числа электронов, отдаваемых металлом и присоединяющихся к окислителю в единицу времени. Только в этом случае может наступить стационарное состояние. Итак, процессы электрохимической коррозии протекают по законам электрохимической кинетики, когда общая реакция взаимодействия может быть разделена на следующие, в значительной степени самостоятельные, электродные процессы: – анодный процесс – переход металла в раствор в виде ионов (в водных растворах, обычно гидратированных) с оставлением эквивалентного количества электронов в металле: Ме 0 – nē → Ме n+ – катодный процесс – ассимиляция появившихся в металле избыточных электронов деполяризаторами. Различают коррозию с водородной и кислородной (или окислительной) деполяризацией. При наличии в растворе газообразного кислорода и невозможностью протекания процесса коррозии с водородной деполяризацией основную роль деполяризатора исполняет кислород. Коррозионные процессы, у которых катодная деполяризация осуществляется растворенным в электролите кислородом, называют процессами коррозии металлов с кислородной деполяризацией. Это наиболее распространенный тип коррозии металла в воде, в нейтральных и даже в слабокислых солевых растворах, в морской воде, в земле, в атмосфере воздуха. Общая схема кислородной деполяризации сводится к восстановлению молекулярного кислорода до иона гидроокисла: O + 4ē +2h3O → 4OH—. В случае водородной деполяризации на катоде протекает процесс восстановления ионов водорода, находящихся в среде: 2Н++ 2ē + → Н2. Выбор того или иного способа определяется его эффективностью, а также экономической целесообразностью. 2.3.1 Легирование металла – эффективный (хотя обычно дорогой) метод повышения коррозионной стойкости металлов. При легировании в состав сплава обычно вводят компоненты, вызывающие пассивирование металла. В качестве таких компонентов применяются хром, никель, вольфрам и др. Основное средство защиты металлов от газовой коррозии – легирование такими компонентами, которые улучшают свойства защитных пленок, образующихся при окислении металла. Для стали такими элементами являются хром, алюминий, кремний. Эти элементы при высоких температурах окисляются энергичнее, чем железо, и образуют при этом плотные защитные пленки оксидов. 2.3.2 Защитные покрытия. Слои, искусственно создаваемые на поверхности металлических изделий и сооружений для предохранения их от коррозии, называются защитными покрытиями. Выбор вида покрытия зависит от условий, в которых используется металл. Широко распространенным способом защиты металлов от коррозии является покрытие их слоем других металлов. Покрывающие металлы сами корродируют с малой скоростью, так как покрываются плотной оксидной пленкой. В зависимости от величины электродного потенциала защищаемого металла и покрытия, различают катодные и анодные покрытия. Катодное покрытие – металл покрытия менее активен, чем защищаемый металл. Например, олово хорошо покрывает железо и достаточно стойко против действия разбавленных растворов кислот. В случае механического повреждения такого покрытия возникает гальваническая пара, в которой электроны переходят от железа к олову; анодом здесь является железо, а катодом олово. В этом случае разрушается железо, а олово остается без изменений (рисунок 5). Анодное покрытие – покрытие более активным металлом. Например, покрытие железа цинком (рисунок 4). При механическом повреждении цинкового покрытия возникает гальваническая пара, в которой железо служит катодом, а анодом – цинк. Электроны переходят от цинка к железу, цинк разрушается, а железо остается защищенным до тех пор, пока не разрушится весь цинк. На основании вышеизложенного можно сделать вывод о том, что более надежным является анодное покрытие. а)б) 1 – раствор; 2 – покрытие; 3 – основной материал; 4 – пора Рисунок 4 – Схема коррозии металла в кислом растворе при нарушении анодного а) и катодного б) покрытия К ряду покрытий, получаемых химической обработкой металла, относятся защитные покрытия, образующиеся непосредственно на поверхности металла. Образование на поверхности металлических изделий защитных оксидных пленок носит в технике общее название оксидирование. Неметаллические защитные покрытия могут быть как неорганическими, так и органическими. Защитное действие этих покрытий сводится в основном к изоляции металла от окружающей среды. В качестве неорганических покрытий могут быть неорганические эмали, оксиды металлов, соединения хрома, фосфора и др. К органическим относятся лакокрасочные покрытия, покрытия смолами, пластмассами, полимерными пленками, резиной. 2.3.3 Электрохимические методы защиты. Методы электрохимической защиты основаны на изменении потенциала защищаемого металла и не связаны с изоляцией металла от коррозионной среды. К ним относятся катодная защита, называемая также электрозащитой, и протекторная (или анодная) защита. Катодная защита заключается в том, что защищаемая конструкция А (рисунок 5), находящаяся в среде электролита (например, в почвенной воде), присоединяется к катоду внешнего источника электричества В. Защищаемая конструкция становится катодом. В ту же агрессивную среду помещают кусок старого металла Б (рельс, балка), присоединяемый к аноду внешнего источника электричества. В процессе коррозии этот кусок старого металла становится анодом и разрушается. Протекторная защита отличается от катодной защиты тем, что для ее осуществления используется специальный анод – протектор, в качестве которого применяют металл более активный, чем металл защищаемой конструкции (алюминий, цинк). Протектор Б (рисунок 6) соединяют с защищаемой конструкцией А проводником электрического тока В. В процессе коррозии протектор служит анодом и разрушается, тем самым предохраняя от разрушения защищаемую конструкцию. Рисунок 5 – Схема катодной Рисунок 6 – Схема анодной защиты (протекторной) защиты 2.3.4 Изменение свойств коррозионной среды. Изменение свойств коррозионной среды пригодно для случаев, когда защищаемое изделие эксплуатируется в ограниченном объеме жидкости. Один из методов состоит в удалении из раствора, в котором эксплуатируется защищаемая деталь, растворенного кислорода (деаэрация). В качестве примера можно привести освобождение воды, идущей на питание паровых котлов, от растворенного в ней кислорода, что достигается, например, при фильтровании воды через слой железных стружек. Для замедления коррозии металлических изделий в агрессивную среду вводят вещества, называемые ингибиторами (или замедлителями) коррозии. Это имеет большое значение в тех случаях, когда металл необходимо защищать от разъедания кислотами. В зависимости от вида коррозии, природы металла и раствора применяются различные ингибиторы, действие которых специфично. 2.3.5 Создание рациональных конструкций. Выбор материалов и их сочетаний для данной машины, конечно, диктуется технической и экономической целесообразностью, но должен обеспечивать ее коррозионную устойчивость. Конструктор должен предусмотреть рациональные формы машины, допускающие быструю очистку от грязи; машина не должна иметь мест скопления влаги, которая является возбудителем коррозии. studfiles.net Электрохимическая коррозия – это наиболее распространенный тип нарушения целостности металлической структуры. При этом не обязательно погружение детали в электролит. Часто бывает достаточно наличия тонкой пленки на поверхности материала. Электрохимическая коррозия металлов происходит, в большей степени, в результате повсеместного применения технической и бытовой соли (хлорид калия и натрия). Чаще всего эти вещества используют в зимний период для быстрого устранения льда и снега с улиц городов. Больше всего, как показывает практика, ущерба таким образом наносится подземным коммуникациям и наземному транспорту. Электрохимическая коррозия наблюдается на деталях машин, конструкций, приборов, находящихся в условиях почвы, грунта, воды (морской или речной), атмосферы, в растворах технического назначения, под воздействием смазочных, охлаждающих продуктов. Разрушение могут спровоцировать блуждающие токи, которые возникают при утечке части тока из электрической цепи в почву или воду, а оттуда – в элементы конструкций. Там, где происходит обратный выход (из металлов в почву или воду) отмечается разрушение деталей – электрохимическая коррозия. Чаще всего блуждающие токи формируются в местах, где движется наземный транспорт (трамваи, железнодорожные локомотивы на электрической тяге). При этом, как показывают исследования, 1 Ампер за год способен растворить 33,4 кг свинца, 10,7 кг цинка и 9,1 кг железа. Часто в развитии разрушения участвует несколько факторов. Электрохимическая коррозия представляет собой особый процесс. Сплав (или самостоятельный материал) утрачивает часть имеющихся атомов. Они (атомы) переходят в виде ионов в электролитический раствор. Вместо утраченных металлом частиц появляются электроны, которые заряжают материал отрицательным зарядом. При этом электролит обладает зарядом положительным. Таким образом, электрохимическая коррозия формирует гальваническую пару. Окислительно-восстановительным реакциям в большей степени способствует неоднородность в химической структуре материала. Провоцирующими факторами в формировании анодов и катодов являются и участки остаточной деформации, отсутствие однородности в покрывающих металл защитных пленках. Пронаблюдать разрушение деталей можно и в домашних условиях. Для этого потребуются три гвоздя, три стакана с солевым раствором (пищевая соль, растворенная в воде), небольшой кусочек цинка, медная проволока (изоляцию следует устранить). Первый гвоздь опускается в стакан с солевой смесью. Ко второму следует прикрутить проволоку и также поместить в раствор (во второй стакан). Третий гвоздь опускается в третью емкость. Оставить на двое-трое суток. По истечении этого периода на всех трех гвоздях будет отмечаться ржавчина. Однако в самом плохом состоянии будет гвоздь с проволокой, в лучшем – с цинком. Такая разница связана с различной способностью металлов отдавать электроны. Для защиты материала применяют метод изменения его потенциала. Следует отметить, что методика не связана с изоляцией. В качестве защиты применяют катодный (анодный) метод. При этом защищаемую конструкцию, находящуюся в неблагоприятной (например, в почвенной) среде, присоединяют к катоду (заряженному отрицательно электроду) электрического источника. Таким образом, деталь становится катодом. В эту же среду помещают и старую деталь, присоединяя ее к аноду от внешнего источника. Коррозийный процесс приводит к разрушению старого металла, который становится анодом. Существует также и протекторный тип защиты. В отличие от описанного выше, этот вариант предусматривает применение особого анода – протектора. В его качестве используют более активный, нежели у защищаемой конструкции, металл. В процессе коррозийного разрушения протектор выполняет задачу анода (положительного электрода) и, разрушаясь, предохраняет от нарушения целостности в охраняемой детали. fb.ru Электрохимическая коррозия металла может проявиться в тех случаях, когда имеет место граница раздела фаз металл-электролит. Факт проявления коррозии не зависит от природы электролита, будь это сверхчистая вода или расплавленная соль. Не имеет существенного значения и количество электролита - в предельном случае это может быть пленка влаги толщиной в несколько десятков миллимикрон. Схема процесса коррозии.Анодный процесс при коррозии всегда заключается в ионизации металла. Металл переходит в раствор в виде гидратированных ионов, при этом в металле остается соответствующее число электронов. Примерами анодных реакций могут быть: Fe - 2ē = Fe2+ - окисление железа Al - 3ē = Al3+- окисление алюминия В общей форме реакция выглядит так: Me – nē = Men+, где Me - металл. Катодный процесс - поглощение появившихся в металле избыточных электронов с помощью так называемых деполяризаторов, которыми могут являться атомы, молекулы, ионы раствора, подвергающиеся восстановлению на всей поверхности металла или отдельных ее участках. Примерами катодных реакций могут быть следующие: 2Н+ + 2ē → 2Н → Н2 - восстановление ионов водорода в кислой среде. О2 + 4Н+ + 4ē → 2Н2О - восстановление растворенного кислорода в кислой среде. О2+2Н2О + 4ē → 4ОН-- восстановление растворенного кислорода в нейтральной или щелочной среде. В общей форме уравнение катодной реакции выглядит так: D + ē → D, где D – деполяризатор. Поляризация и ее виды. Коррозия металлов с кислородной и водородной деполяризацией.При прохождении через электрод электрического тока извне происходит смещение его потенциала. Численная величина изменения потенциала вследствие прохождения тока называется поляризацией. Причина возникновения поляризации состоит в том, что переход зарядов из металла в раствор и перемещение ионов в электролите встречают определенное сопротивление. В зависимости от вызывающих его факторов различают три вида по- ляризации: концентрационную, активационную и оммическую. Причиной концентрационной поляризации является разность концентраций ионов в приэлектродном пространстве, следствием чего является изменение потенциала электрода. Возникновение активационной поляризации обусловлено сопротивлением, возникающим во время катодной реакции присоединения электронов деполяризатором или торможением при переходе катионов из металлической решетки в раствор. В электрохимии эти процессы называют стадиями, считается, что самая замедленная стадия определяет скорость процесса. Преодоление такого сопротивления требует добавочной активационной энергии, поэтому и поляризация называется активационной. Омической поляризацией называется падение потенциала JR, вызываемое электрическим сопротивлением слоя электролита вблизи электрода или слоя продуктов реакции, а также обоих этих слоев одновременно. В зависимости от направления сдвига потенциала электрода при прохождении постоянного тока различает анодную и катодную поляризации. Анодной поляризацией называется сдвиг потенциала в положительную сторону, катодной поляризацией - его перемещение в отрицательную сторону. На практике всегда стремятся к увеличению поляризации в коррозионном элементе. Благодаря поляризации металлов скорость коррозии уменьшается в сотни, а то и в тысячи раз. Явление, противодействующее поляризации электрода, принято называть деполяризацией. Деполяризация (анодная и катодная) ускоряет процесс коррозии. Среди большого количества реакций катодной поляризации в коррозионных процессах наибольшее значение имеют реакции, в которых в роли, деполяризатора выступает кислород (кислородная деполяризация) или ионы водорода: водородная поляризация). С водородной деполяризацией протекает коррозия всех металлов, стоящих левее водорода в ряду напряжений, в кислых средах. В нейтральных средах с водородной деполяризацией протекает коррозия активных металлов, а в щелочных средах - амфотерных металлов. С кислородной деполяризацией протекает коррозия металлов малой и средней активности в нейтральных средах и в любых средах металлов малой активности, т.е. стоящих в ряду напряжений после водорода. С кислородной деполяризацией протекает атмосферная и почвенная коррозия. Существенное влияние на скорость коррозии оказывает скорость доставки кислорода к металлу путем диффузии или конвекции, а также такие факторы как перемешивание электролита, глубина погружения корродирующего металла, растворимость кислорода в растворе и т.д. Причины возникновения гальванопар.В процессах электрохимической коррозии можно выделить следующие типы возникновения гальванических пар (т.е. разности потенциалов на поверхности металлов): 1. Практически любой металл содержит примеси других металлов или соединения того же металла. В среде электролита система из основного металла и металла примеси образует большое число гальванопар. Участки с более электроотрицательными потенциалами окажутся анодами (по отношению к внутреннему участку цепи) и будут растворяться, a нa более электроположительных участках (катодах) будут происходить процессы восстановления. Таким образом, одной из причин электрохимической коррозии является возникновение микро - и макрогальваничесхих элементов на поверхности металла. На рис. 69 представлена схема коррозии железа с включением меди. Рис.69. Схема коррозии железа с включением меди Электрохимическая система этой гальванопары в электролите изображается, как и в случае гальванического элемента, схемой A (-) Fe│h3SO4│Cu (+) K железо - анод, медь - катод На аноде: Fe - 2ē = Fe2+ На катоде: 2Н+ + 2ē = Н2 В результате железо разрушается в месте контакта, а на меди выделяется водород. 2. Гальванопары могут возникать и в результате неравномерности аэрации, т.е. неравномерного доступа кислорода к различным участкам поверхности металла. На рис. 70 показана схема коррозии железа при неравномерном доступе кислорода. Участки поверхности металла, к которым быстрее диффундирует кислород - катодные, к которым затрудняется доступ кислорода – анодные. На аноде: Fe - 2ē = Fe2+ На катоде: O2 + 2Н2O + 4ē = 4ОН- (в нейтральной среде) Рис. 70. Схема коррозии железа при неравномерной аэрации В ходе коррозии химический состав раствора вблизи металлической поверхности подвергается непрерывным изменениям. Результатом этих изменений являются вторичные реакции. Из приведенной выше схемы видно, что вблизи катодного участка происходит подщелачивание и ионы железа могут вступить в реакцию с ионами OН- с образованием гидроокиси железа: Fe2+ + 2OH- → Fe (OH)2 Труднорастворимая гидроокись железа выпадает в осадок. Если процесс протекает в воздушной среде, то гидроокись железа (II) окисляется кислородом воздуха в гидроокись железа (III): 4Fe (OH)2 + O2 + 2h3O → 4Fe (OH)3 Гидроксиды железа неустойчивы и постепенно могут переходить в соответствующие оксиды. Продукты электрохимической коррозии железа, состоящие из гидратированных оксидов, называются ржавчиной. 3. Возникновение разности потенциалов может наблюдаться для одного и того же металла, части которого контактируют с электролитом разной концентрации. В растворе с меньшей концентрацией поверхность металла заряжается отрицательно (анод), а в более концентрированном растворе - положительно (катод). 4. Часто детали изделия, выполненные из одного и того же металла и различающиеся только по температуре эксплуатации могут подвергаться электрохимической коррозии. Такие контакты встречаются в промышленных устройствах, соприкасающихся с нагретыми газами или жидкостями, например, в паровых котлах, змеевиках и т.д. 5. Различный уровень механических напряжений в одной и той же детали приводит к возникновению микрогальванопар. Если согнутая металлическая пластинка погружена в коррозионную среду, то на растянутом слое через некоторое время начнут возникать трещины (анод), внутренний слой останется без изменения (катод). Факторы, влияющие на коррозию.На скорость коррозии влияют различные факторы: природа металла, его структу- ра и состояние поверхности, химический состав и свойства среды, температура электролита, природа поверхностных оксидных пленок, условия работы изделия, влажность, пыль и др. Например, состав электролита определяет электропроводность и активную концентрацию ионов, участвующих в процессе. Ускоряют коррозионные процессы во всех случаях и для всех металлов ионы Н+, Сl-, Br-, I-, понижая потенциал растворения металлов. Для амфотерных металлов такую роль играют ионы ОН-. Присутствие в электролите ионов или полярных молекул, которые могут выступать как лиганды при комплексообразовании и растворять пассивирующие пленки (Сl -, СN -, Nh4), значительно ускоряет коррозионные процессы. С увеличением температуры скорость коррозии металлов, как правило, возрастает, причем эта зависимость носит экспоненциальный характер. Скорость коррозии стали в НСl, идущая с выделением водорода, удваивается при увеличении температуры на 10°. Однако часто зависимость скорости коррозии от температуры имеет сложный характер (например, в случае, когда процесс коррозии протекает с кислородной деполяризацией). Такое явление наблюдается при коррозии стали в природных водах. 2.2 Электрохимическая коррозия металлов. Что такое электрохимическая коррозия
2.2 Электрохимическая коррозия металлов
2.3Способы защиты от коррозии
Электрохимическая коррозия
Электрохимическая коррозия

Похожие статьи:
poznayka.org
Электрохимическая коррозия — Мегаобучалка
Коррозия и методы защиты от нее
Корро́зия, ржавление, ржа — это самопроизвольное разрушение металлов в результате химического или физико-химического взаимодействия с окружающей средой. В общем случае это разрушение любого материала, будь то металл или керамика, дерево или полимер. Причиной коррозии служит термодинамическая неустойчивость конструкционных материалов к воздействию веществ, находящихся в контактирующей с ними среде. Пример — кислородная коррозия железа в воде:
Гидроксид железа и является тем, что называют ржавчиной.
В повседневной жизни для сплавов железа (сталей) чаще используют термин «ржавление». Менее известны случаи коррозии полимеров. Применительно к ним существует понятие «старение», аналогичное термину «коррозия» для металлов. Например, старение резины из-за взаимодействия с кислородом воздуха или разрушение некоторых пластиков под воздействием атмосферных осадков, а также биологическая коррозия. Скорость коррозии, как и всякой химической реакции, очень сильно зависит от температуры. Повышение температуры на 100 градусов может увеличить скорость коррозии на несколько порядков.
Классификация видов коррозии
Коррозионные процессы отличаются широким распространением и разнообразием условий и сред, в которых они протекают. Поэтому пока нет единой и всеобъемлющей классификации встречающихся случаев коррозии.
По типу агрессивных сред, в которых протекает процесс разрушения, коррозия может быть следующих видов:
· газовая коррозия;
· атмосферная коррозия;
· коррозия в неэлектролитах;
· коррозия в электролитах;
· подземная коррозия;
· биокоррозия;
· коррозия под воздействием блуждающих токов.
По условиям протекания коррозионного процесса различаются следующие виды:
· контактная коррозия;
· щелевая коррозия;
· коррозия при неполном погружении;
· коррозия при полном погружении;
· коррозия при переменном погружении;
· коррозия при трении;
· межкристаллитная коррозия;
· коррозия под напряжением.
По характеру разрушения:
· сплошная коррозия, охватывающая всю поверхность:
o равномерная;
o неравномерная;
o избирательная;
· локальная (местная) коррозия, охватывающая отдельные участки:
o пятнами;
o язвенная;
o точечная;
o сквозная;
o межкристаллитная (расслаивающая в деформированных заготовках и ножевая в сварных соединениях).
Главная классификация производится по механизму протекания процесса. Различают два вида:
· химическую коррозию;
· электрохимическую коррозию.
Коррозия неметаллических материалов
По мере ужесточения условий эксплуатации (повышение температуры, механических напряжений, агрессивности среды и др.) и неметаллические материалы подвержены действию среды. В связи с чем термин «коррозия» стал применяться и по отношению к этим материалам, например «коррозия бетонов и железобетонов», «коррозия пластмасс и резин». При этом имеется в виду их разрушение и потеря эксплуатационных свойств в результате химического или физико-химического взаимодействия с окружающей средой. Но следует учитывать, что механизмы и кинетика процессов для неметаллов и металлов будут разными.
Коррозия металлов
Коррозия металлов — разрушение металлов вследствие химического или электрохимического взаимодействия их с коррозионной средой. Для процесса коррозии следует применять термин «коррозионный процесс», а для результата процесса — «коррозионное разрушение». Образование гальванических пар с пользой применяют для создания батарей и аккумуляторов. С другой стороны, образование такой пары приводит к неблагоприятному процессу, жертвой которого становится целый ряд металлов, — коррозии. Под коррозией понимают происходящее на поверхности электрохимическое или химическое разрушение металлического материала. Наиболее часто при коррозии металл окисляется с образованием ионов металла, которые при дальнейших превращениях дают различные продукты коррозии. Коррозия может быть вызвана как химическим, так и электрохимическим процессом. Соответственно, различают химическую и электрохимическую коррозию металлов.
Типы коррозии
Различают 4 основных вида коррозии: электрохимическая коррозия, водородная, кислородная коррозия и химическая.
1.
a)
В некоторых металлах (Zn) катионы легко переходят в раствор; пластины заряжаются отрицательно, а раствор положительно.
б)
Катионы в растворе легко теряют гидратные оболочки и адсорбируются на поверхность металлов: металл +, раствор -.
Вывод: Металлы (рис. а) являются анодами по отношению к водородному электроду, а (рис. б) катодами.
Потенциалы газовых электродовГазовые электроды могут быть обратимыми относительно анионов (кислородный) или относительно катионов (водородный). Газовые электроды состоят из металлического проводника, контактирующего одновременно с газом и раствором, содержащим ионы этого газа. Металлический проводник служит для подвода и отвода электронов и, кроме того, является катализатором электродной реакции (ускоряет установление равновесия на электроде). Металлический проводник не должен посылать в раствор собственные ионы, т.е. быть инертным, а также обладать хорошей адсорбционной способностью, так как в электродном процессе участвуют адсорбированный газ и его ионы в растворе. Всем этим требованиям удовлетворяют платина, покрытая электролитическим способом платиновой чернью, и металлы платиновой группы, поэтому они чаще всего используются при создании газовых электродов.
Так как в равновесных электродных реакциях газовых электродов участвуют газообразные компоненты, то потенциалы этих электродов зависят от парциальных давлений газов.
Потенциал водородного электрода зависит от РН.
Кислородный электрод:
Потенциал кислородного электрода так же изменяется при изменении
Электрохимическая коррозия
- наиболее распространенный вид коррозии металлов, это разрушение металла в среде электролита с возникновением внутри системы электрического тока. Примером коррозионных процессов электрохимического характера является разрушение деталей машин и различных металлических конструкций в почвенных, грунтовых, речных и морских водах, во влажной атмосфере, в технических растворах, под действием смазочно-охлаждающих жидкостей, применяемых при механической обработке металлов и т.д.
Причиной электрохимической коррозии является образование на поверхности металла большого количества микрогальванических пар, которые возникают по следующим причинам:
1. Наличие примесей металлов или других веществ, отличающихся по активности от основного металла.
2. Структурная неоднородность поверхности металла, что определяет наличие участков с разной активностью.
3. Неравномерность распределения деформаций в металле после термической и механической обработки и др.
При электрохимической коррозии на поверхности металла одновременно протекают два процесса:
анодный - окисление металла:
и катодный - восстановление ионов водорода в кислой среде:
или
молекул кислорода, растворенного в воде, в случае атмосферной коррозии:
Не следует путать электрохимическую коррозию с электрохимической коррозией однородного материала, например, ржавление железа или т. п. При электрохимической коррозии (наиболее частая форма коррозии) всегда требуется наличие электролита (Конденсат, дождевая вода и т. д.), с которым соприкасаются электроды — либо различные элементы структуры материала, либо два различных соприкасающихся материала с различающимися окислительно-восстановительными потенциалами. Если в воде растворены ионы солей, кислот, или т. п., электропроводность её повышается, и скорость процесса увеличивается.
Коррозионный элемент
При соприкосновении двух металлов с различными окислительно-восстановительными потенциалами и погружении их в раствор электролита, например, дождевой воды с растворенным углекислым газом CO2, образуется гальванический элемент, так называемый коррозионный элемент. Он представляет собой не что иное, как замкнутую гальваническую ячейку. В ней происходит медленное растворение металлического материала с более низким окислительно-восстановительным потенциалом; второй электрод в паре, как правило, не корродирует. Этот вид коррозии особо присущ металлам с высокими отрицательными потенциалами. Так, совсем небольшого количества примеси на поверхности металла с большим редокспотенциалом уже достаточно для возникновения коррозионного элемента. Особо подвержены риску места соприкосновения металлов с различными потенциалами, например, сварочные швы или заклёпки.
Гальвани́ческий элеме́нт — химический источник электрического тока, основанный на взаимодействии двух металлов и/или их оксидов в электролите, приводящем к возникновению в замкнутой цепи электрического тока. Назван в честь Луиджи Гальвани. Переход химической энергии в электрическую энергию происходит в гальванических элементах.
| Гальванический элемент | Микрогальванический элемент |
| Анод-металл с меньшим значением электронного потенциала, катод- с большим. | |
| Перенос электронов проискходит по внешней цепи. | Перенос электронов происходит внутри пластины. |
| Ионы перемещаются через ключ. | Ионы перемещаются по раствору электролита. |
Для гальванического элемента принята следующая форма записи (на примере элемента Даниэля):
,
где вертикальная линия | обозначает границу раздела фаз, а двойная вертикальная линия - солевой мостик. Электрод, на котором происходит окисление, называется анодом; электрод, на котором происходит восстановление, называется катодом. Гальванический элемент принято записывать так, чтобы анод находился слева.
Электродные полуреакции принято записывать как реакции восстановления (таблица 12.1), поэтому общая реакция в гальваническом элементе записывается как разность между реакциями на правом и левом электродах:
Правый электрод:
Левый электрод:
Общая реакция:
Для защиты железных конструкций от коррозии наиболее часто применяют металлическое покрытие из цинка (оцинкованное железо, жесть) или олова (луженое железо, белая жесть). В первом случае цинк является более активным восстановителем, чем железо, так как Ре Ге2+ = = -0,440 В. Поэтому при нарушении покрытия в коррозионных микрогальванических элементах цинк будет анодом и разрушаться, а железо катодом — местом, для осуществления процессов восстановления окислителей среды. Для описания процессов в этой системе на рис. 38.7 следует слева взять более активный металл — цинк (вместо железа), а справа — менее активный — железо (вместо меди) и заменить ионы железа в среде на ионы цинка. Поскольку в данном процессе цинк является анодом, то цинковое покрытие железа называется анодным покрытием.
Таким образом, электрохимическая коррозия металлов — это результат деятельности микрогальванических элементов на их поверхности.
Микрогальваническими элементами может быть объяснена характерная особенность кинетики взаимодействия металлов с кислотами — в течение довольно длительного начального периода скорость растворения металла и выделения водорода возрастает. Это связано с постепенным накоплением на реакционной поверхности тех включений, которые в начале реакции находились не на поверхности.
Деполяризация
Процесс отвода электронов с катодных участков называется деполяризацией. Вещества, при участии которых осуществляется деполяризация, называются деполяризаторами. На практике чаще всего приходится встречаться с двумя типами деполяризации: водородной и кислородной. Тип деполяризации (катодный процесс) зависит от реакции среды раствора электролита.
В кислой среде электрохимическая коррозия протекает с водородной деполяризацией. Рассмотрим пример коррозии Zn/Fe
В данном случае цинк будет анодом (Zn=-0,76), а железо – катодом (Fe= –0,44). На анодном участке будет происходить:
– окисление
– восстановление
Схема возникающего гальванического элемента выглядит следующим образом:
нейтральной среде коррозия протекает с кислородной деполяризацией, т.е. роль деполяризатора выполняет кислород, растворенный в воде. Этот вид коррозии наиболее широко распространен в природе: он наблюдается при коррозии металлов в воде, почве и в незагрязненной промышленными газами атмосфере. Если коррозии во влажном воздухе подвергается железо с примесями меди, то электродные процессы можно записать в виде:
– окисление
– восстановление
Схема короткозамкнутого гальванического элемента:
У поверхности металла в электролите протекают следующие реакции:
Основная масса черных металлов разрушается вследствие процесса ржавления, в основе которого лежат вышеуказанные реакции.
megaobuchalka.ru
Определение и классификация коррозионных процессов. Химическая и электрохимическая коррозия
При эксплуатации изделий из металлов и их сплавов приходится сталкиваться с явлением разрушения их под действием внешней среды. Разрушение металлов и сплавов вследствие взаимодействия их с окружающей средой называется коррозией.
Коррозия металлов наносит большой экономический ущерб. В результате коррозии выходят из строя оборудование, машины, механизмы, разрушаются металлические конструкции. Особенно сильно подвёргается коррозии оборудованиё, которое контактирует с агрессивными средами, например, растворами кислот, солей.
Коррозионное разрушение может затрагивать всю поверхность металла - сплошная (общая) коррозия, или отдельные участки - местная (локальная) коррозия. В зависимости от механизма процесса различают химическую и электрохимическую химическую коррозию.
Химическая коррозия — это разрушение металла из-за окисления его окислителями, находящимися в коррозионной среде.
Химическая коррозия протекает без возникновения электрического тока в системе. Такой вид коррозии возникает при контакте металлов с неэлектролитами или в газовой среде при высоких температурах (газовая коррозия).
Газовая коррозия встречается довольно часто. С ней мы сталкиваемся при коррозии металлов в печах, выхлопных трубах и т.п. Наиболее опасными для металлов компонентами газовой среды являются кислород, пары воды, оксид углерода (IV), оксид серы (IV). Коррозионное разрушение железа и его сплавов на воздухе обусловлено окислением его кислородом воздуха.
С повышением температуры скорость газовой коррозии возрастает. Наибольший вред приносит электрохимическая коррозия.
Электрохимической коррозией называется разрушение металла при контакте с электролитами с возникновением в системе электрического тока.
Коррозия - это разрушение металлов в результате химической и электрохимической реакции.
Разрушение (порча), происходящие по физическим причинам не называются коррозией, а известно как эрозия или истирание или износ.
Термин "коррозия" относится только к химическому воздействию на металлы и не распространяется на неметаллические материалы. Пластмассы могут набухать, трескаться; дерево - расслаиваться или гнить.
Ржавление - коррозия железа и его сплавов с образованием продуктов коррозии, состоящих в основном из оксидов железа (гидратированных).
Цветные металлы, следовательно, корродируют, но не ржавеют.
Коррозионная наука.
Так как коррозия включает химическое превращение, для лучшего понимания коррозионных реакций необходимо знать основы химии и особенно электрохимии, так как коррозионные процессы по большой части являются электрохимическими.
Так как структура и состав металла зачастую определяют коррозионное поведение, надо быть знакомым с основами металлургии. Следовательно, химия и металлургия составляют фундамент при изучении коррозии, так же как биология и химия - при изучении медицины.
Коррозионная проблема.
Значение коррозионных исследований определяется тремя аспектами:
1 . Экономический.
Имеет целью уменьшение материальных потерь в результате коррозии трубопроводов, котлов, судов, мостов.
2. Повышение надежности оборудования.
Оборудование в результате коррозии разрушается с катастрофическими последствиями, например: сосуд высокого давления, паровые котлы, контейнера для токсичных материалов.
3. Сохранность металлического фонда.
Мировые ресурсы металла ограниченны, а потери в результате коррозии ведут к дополнительным затратам энергии и воды. И человеческий труд, затрачиваемый на проектирование и реконструкцию.
Причины коррозии металлов:
В природе все металлы (за исключением золота, серебра, металлов платиновой группы и в меньшей степени медь и ртуть) в основном встречаются в виде минералов, таких как сульфиды, силикаты, карбонаты. Для извлечения металла минерал необходимо подвергнуть реакции восстановления, используя в качестве восстановителя какое-либо вещество
 |
.
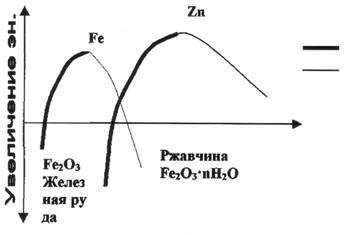
Химическое восстановление
Коррозия
Рис 1. Изменение во времени химической энергии при восстановлении оксидов в металлы и в ходе обратной реакции коррозии
2Fе2О3 + ЗС  4Fе + ЗСО2 (гематит)
4Fе + ЗСО2 (гематит)
2ZnО + С  2Zn + СО2
2Zn + СО2
Из графика (рис.1) видно, что металлический Zn энергетически менее стабилен, чем Fе и в атмосферных условиях имеет тенденцию превращаться в сложную смесь из гидроксида и основного карбоната и т.п. Однако, если ржавчина, образующаяся на стали представляет собой рыхлую массу, почти не защищает поверхность металла от проникновения Н2О и О2, то продукты коррозии Zn обладают существенными защитными свойствами, благодаря чему Zn коррозирует медленнее, чем Fе. По этой причине мягкие стали защищают Zn покрытием.
Типы коррозионных разрушений:
I. По характеру изменения поверхности металла или степени изменения физико-механических свойств.
Различают 5 основных типов коррозии:
1. Равномерная (общая или сплошная) - ржавление железа или потускнение серебра, высокотемпературное окисление металлов.
Скорость равномерной коррозии выражают в разных единицах мм/год или г/м2сутки. Например, сталь в морской воде коррозирует с постоянной скоростью ~ 0,13 мм/год, т.е. 2,5 г/м2сутки.
2. Местная коррозия - разрушение отдельных участков поверхности металла. Она имеет неодинаковую степень разрушения. Наиболее характерными видами местной коррозии являются коррозия в виде пятен, язв, точечная, межкристаллическая. Местная коррозия бывает трех типов:
а) точечная (питинг) - разрушает металл в виде отдельных точечных поражений, перерастающих в сквозные (коррозия нержавеющей стали в морской воде).
 |
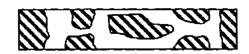 б) межкристаллическая коррозия (МКК) - это разрушение на границах зерен, приводящие к потери прочности и пластичности
б) межкристаллическая коррозия (МКК) - это разрушение на границах зерен, приводящие к потери прочности и пластичности
Межзеренное вещество, действующее как анод, контактирующее с большой поверхностью самих зерен, являющейся катодом. Коррозия протекает быстро, глубоко проникая в металл и приводя иногда к катастрофическим разрушениям. Нержавеющие стали или дюраль подвергнутые неправильной термообработке, склонны к (МКК) в зонах сварки.
в) транскристаллитная - рассекающая металл трещиной прямо через зерна. Растрескивание металла под действием периодических или растягивающих напряжений в коррозионной среде называют коррозионной усталостью.
3. Избирательная - коррозия, которой подвержены сплавы, содержащие несколько структурных составляющих.
4. Обесцинкование - это вид разрушения цинковых сплавов, например латуни, при котором преимущественно корродирует цинк, а медь остается на поверхности в виде пористого слоя. Прокорродировавшее, таким образом, изделие нередко сохраняет исходную форму и может показаться не поврежденными, но его прочность и особенно пластичность значительно снижены.
Подвергшаяся обесцинкованию латунная труба способна выдерживать внутреннее давление воды, однако разрушиться при гидравлическом ударе или проведении ремонтных работ.
5. Разрушение окисных пленок на поверхности металлов. При повреждении пленки А12Оз на алюминиевом изделии, находящемся в морской воде, возникает электролит 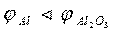 .
.
 |
Различные внутренние механические напряжения 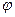 напр. <
напр. < 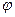 ненапр. Поэтому в первую очередь будут растворяться напряженные участки металла. Внутренние напряжения в металлах существенно изменяются при сварочных работах. Уменьшить эти напряжения можно термообработкой изделия.
ненапр. Поэтому в первую очередь будут растворяться напряженные участки металла. Внутренние напряжения в металлах существенно изменяются при сварочных работах. Уменьшить эти напряжения можно термообработкой изделия.
II. По механизму реакции взаимодействия с окружающей средой различают:
1. Химическую.
2. Электрохимическую.
Особо выделяют биологическую коррозию идущую под влиянием продуктов жизнедеятельности бактерий и микроорганизмов и радиационную коррозию, протекающую под воздействием радиоактивного излучения.
Электрохимическая коррозия - это разрушение металлов и сплавов под действием жидкостей электролита. Электрохимическая коррозия осуществляется как гальванический процесс за счет разности электрохимических потенциалов различных частей изделия, если оно сделано из разных металлов или за счет разности потенциалов различных участков поверхности одного и того же металла, если он находится в различных концентрациях электролита.
В этом случае наряду с химическими процессами (отдача электронов) протекают и электрические (перенос электронов от одного участка к другому). При этом в результате взаимодействия металла с молекулами воды из коррозионной среды на нем протекают два процесса: окисление металла Ме (анодный процесс) и восстановление окислителей — компонентов среды (катодный процесс). Как правило, в качестве окислителей выступают ионы водорода (коррозия с водородной деполяризацией) или растворенный в воде кислород (коррозия с кислородной деполяризацией). В первом случае при катодном процессе выделяется водород, а во втором образуются гидроксид ионы. Участки поверхности металла, на которых протекают процессы окисления и восстановления, называют соответственно, анодными и катодными. Далее рассмотрим условия, при которых возможно протекание электрохимической коррозии.
Условия возникновения электрохимической коррозии:
1. Контакт двух металлов в электролите.
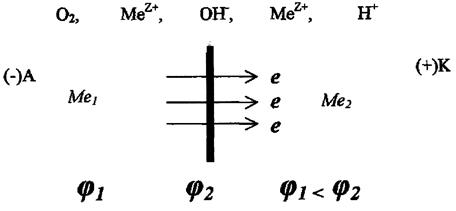 |
А: Ме1° - 2е  Ме
Ме 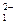
К: 1) 2Н++ 2е  Н2, если рН < 7 (среда кислая)
Н2, если рН < 7 (среда кислая)
2) О2 + 2Н2О + 4е  4ОН
4ОН 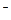 (среда нейтральная)
(среда нейтральная)
При контакте двух разнородных металлов образуется гальванопара в которой разрушается более активный металл. Наибольшая коррозия вблизи места контакта и по мере удаления ослабевает. При этом большую роль играет электропроводность среды. Интенсивность коррозии зависит от разности потенциалов между металлами более активный разрушается тем быстрее, чем больше разность потенциалов контактирующих металлов. Большое влияние оказывает соотношение площадей контактирующих поверхностей. Это связано с тем, что V коррозии определяется не только силой тока, но и плотностью тока (i) i=I/S. Поэтому опасно такое сочетание металла, при котором анод имеет малую площадь, а катод большую (Sан< Sкат). В этом случае анод малой площадью корродирует очень интенсивно.
Для разработки мероприятий по защите конструкций от контактной коррозии необходимо руководствоваться ГОСТ 9.005-92 "Машины, приборы и другие технические изделия. Допустимые и недопустимые контакты металлов"
При выборе металла должны учитывать:
1. Потенциал, площадь поверхности;
2. Между деталями из разнородных металлов нужно использовать, где это возможно изолирующие прокладки, мастики, герметики;
3. На контакт сопрягаемых деталей следует наносить изолирующее покрытие.
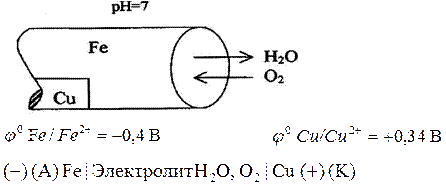
Анод: Fе° - 2е  Fе2+
Fе2+
Катод: О2 + 4е + 2Н2О  4ОН
4ОН 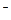
2Fе + О2 + 2Н20  2Fе(ОН)2
2Fе(ОН)2
4Fе(ОН)2 + О2 + 2Н2О  4Fе(ОН)3
4Fе(ОН)3
ржавчина Fе(ОН)2 Fе(ОН)3 FеООН 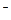
2. Различная аэрация (омывание газами).
То есть это различный доступ кислорода к одной и той же детали, такая коррозия встречается по ватерлинии судов.
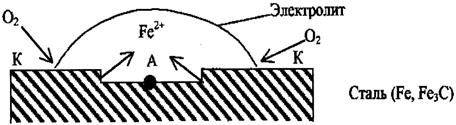 |
А: Fе° - 2е  FеC
FеC
К: О2 + 4е + 2Н2О  4ОН
4ОН 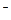
В центре капли, куда доступ кислорода мал, разрушается сам металл (становится эта часть поверхности анодом). По периферии, где проникновение О2 будет большим, он адсорбируется на поверхности металла и защищает его от действия электролита.
Вещества, принимающие на катоде электроны, называются деполяризаторами (вещества уменьшающие поляризацию) т.е. в данном случае кислород является деполяризатором. Наличие деполяризаторов усиливает коррозию. В качестве деполяризаторов могут быть и ионы водорода, которые при этом восстанавливаются. Поэтому понижение рН (подкисление) усиливает процесс коррозии.
3. Неоднородность поверхности металла.
Неоднородность поверхности металла возникает в результате:
а) повреждения оксидной пленки при изгибе, прессовании.
А: А1 - Зе  А1
А1 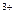 А: Fе - 2е
А: Fе - 2е  Fе2+(кислая среда)
Fе2+(кислая среда)
К: 2Н++ 2е  Н
Н  К: 2Н++ 2е
К: 2Н++ 2е  Н
Н 
Коррозия с водородной деполяризацией, наличие деполяризатора для коррозии вредно. Оксидная пленка разрушается еще ионами NО3-, SО4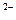 , Сl
, Сl 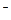 -ионы активаторы.
-ионы активаторы.
(-)А1 | Морская вода, О2 | А12О3 (+)
(-)А: А1 - Зе  А1
А1 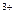
(+)К: О2 + 2Н2О + 4е  4ОН
4ОН 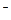
4А1 + ЗО2 + 6Н2О  4А1(ОН)3
4А1(ОН)3
б) Неоднородность металлов и сплавов.
Рассмотрим, контакт двух форм стали, цементита (Fе3С) со
значительным содержанием углерода и перлита с меньшим содержанием углерода. В связи с тем, что потенциал перлита меньше потенциала цементита, в образовавшемся гальваническом элементе протекают реакции. Содержание углерода может уменьшаться в около шовной зоне после сварки.
(-)перлит | морская вода | цементит (+)
(+) анод Fе° - 2е 
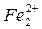
катод О2 + 4е + 2Н2О  4ОН
4ОН 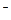
2Fе + О2 + 2Н2О  2Fе(ОН)2
2Fе(ОН)2
в) Неоднородная обработка металла.
Плохо обработанная поверхность металла – анод, хорошо обработанная - катод. Поэтому, изделия находящиеся в агрессивных средах, должны иметь одинаковую обработку поверхности.
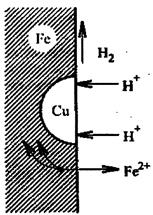 Электрохимическая коррозия может быть усилена, если металл содержит примеси других веществ или неметаллические включения. Например, железо загрязнено примесями меди. При этом возникают гальванические микроэлементы (пары), схема действия которой показана на рис. Металл с более отрицательным потенциалом разрушается — ионы его переходят в раствор, а электроны переходят к менее активному металлу, на котором происходит восстановление ионов водорода (водородная деполяризация) или восстановление растворенного в воде кислорода (кислородная деполяризация) (рис.2).
Электрохимическая коррозия может быть усилена, если металл содержит примеси других веществ или неметаллические включения. Например, железо загрязнено примесями меди. При этом возникают гальванические микроэлементы (пары), схема действия которой показана на рис. Металл с более отрицательным потенциалом разрушается — ионы его переходят в раствор, а электроны переходят к менее активному металлу, на котором происходит восстановление ионов водорода (водородная деполяризация) или восстановление растворенного в воде кислорода (кислородная деполяризация) (рис.2).
|
Таким образом, при электрохимической коррозии (как в случае контакта разнородных металлов, так и случае образования микрогальванических элементов на поверхности одного металла) поток электронов направлен от более активного металла к менее активному (проводнику), и более активный металл корродирует. Скорость коррозии тем больше, чем дальше расположены друг от друга в ряду стандартных электродных потенциалов те металлы, из которых образовался гальванический элемент (гальваническая пара).
На скорость коррозии влияет и характер раствора электролита. Чем выше его кислотность (т. е. меньше рН), а также чем больше содержание в нем окислителей, тем быстрее протекает коррозия. Значительно возрастает коррозия с ростом температуры.
Некоторые металлы при соприкосновении с кислородом воздуха или в агрессивной среде переходят в пассивное состояние, при котором резко замедляется коррозия. Например, концентрированная азотная кислота легко делает пассивным железо, и оно практически не реагирует с концентрированной азотной кислотой. В таких случаях на поверхности металла образуется плотная защитная оксидная пленка, которая препятствует контакту металла со средой. Переход металла в пассивное состояние чаще объясняется образованием на его поверхности хемосорбированного слоя атомов кислорода. При этом атомы кислорода могут покрывать как всю поверхность металла, так и часть ее. Пассивации благоприятствуют легирование более легко пассивирующимся металлом, увеличение концентрации пассиваторов около поверхности металла и другие факторы.
Защитная пленка всегда имеется на поверхности алюминия. Подобные пленки в сухом воздухе образуются также на Ве, Сг, Zn, Та, Ni, Сu и других металлах. Кислород является наиболее распространенным пассиватором.
Пассивированием объясняется коррозионная стойкость нержавеющих сталей и сплавов.
В первую очередь будут растворяться напряженные участки металла.
Внутренние напряжения в металлах существенно изменяются при сварочных работах. Уменьшить эти напряжения можно термообработкой изделия.
Похожие статьи:
poznayka.org
Электрохимическая коррозия - это... Что такое Электрохимическая коррозия?
Электрохимическая коррозия Electrochemical corrosion — Электрохимическая коррозия.Коррозия, вызванная потоком электронов между катодной и анодной областями металлической поверхности.
(Источник: «Металлы и сплавы. Справочник.» Под редакцией Ю.П. Солнцева; НПО "Профессионал", НПО "Мир и семья"; Санкт-Петербург, 2003 г.)
.
- Electrochemical corrosion
- Electrochemical discharge machining
Смотреть что такое "Электрохимическая коррозия" в других словарях:
электрохимическая коррозия — Взаимодействие металла с коррозионной средой (раствором электролита), при котором ионизация атомов металла и восстановление окислительной компоненты коррозионной среды протекают не в одном акте и их скорости зависят от электродного потенциала.… … Справочник технического переводчика
Электрохимическая коррозия — 14. Электрохимическая коррозия Взаимодействие металла с коррозионной средой (раствором электролита), при котором ионизация атомов металла и восстановление окислительной компоненты коррозионной среды протекают не в одном акте и их скорости зависят … Словарь-справочник терминов нормативно-технической документации
электрохимическая коррозия — elektrocheminė korozija statusas T sritis chemija apibrėžtis Metalo korozija dėl savaiminės elektrocheminės oksidacijos. atitikmenys: angl. electrochemical corrosion; galvanic corrosion rus. электрохимическая коррозия … Chemijos terminų aiškinamasis žodynas
ЭЛЕКТРОХИМИЧЕСКАЯ КОРРОЗИЯ — коррозия под действием электролита, при которой ионы металла переходят в раствор и происходит перенос электронов к другим участкам поверхности металла. Основным условием для Э. к. является наличие электролита. Э. к. часто наблюдается в… … Словарь по гидрогеологии и инженерной геологии
Коррозия электрохимическая — – взаимодействие металла с коррозионной средой (раствором электролита), при котором ионизация атомов металла и восстановление окислительной компоненты коррозионной среды протекают не в одном акте и их скорости зависят от электродного… … Энциклопедия терминов, определений и пояснений строительных материалов
Коррозия электрохимическая — Электрохимическая коррозия разрушение металла в результате взаимодействия с коррозионной средой (раствором электролита) или под действием тока от внешнего источника... Источник: ИНСТРУКЦИЯ ПО ЗАЩИТЕ ЖЕЛЕЗНОДОРОЖНЫХ ПОДЗЕМНЫХ СООРУЖЕНИЙ ОТ… … Официальная терминология
Коррозия блуждающим током — – электрохимическая коррозия металла под воздействием блуждающего тока. [ГОСТ 5272 68] Рубрика термина: Виды коррозии Рубрики энциклопедии: Абразивное оборудование, Абразивы, Автодороги, Ав … Энциклопедия терминов, определений и пояснений строительных материалов
Коррозия внешним током — – электрохимическая коррозия металла под воздействием тока от внешнего источника. [ГОСТ 5272 68] Рубрика термина: Виды коррозии Рубрики энциклопедии: Абразивное оборудование, Абразивы, Автодороги … Энциклопедия терминов, определений и пояснений строительных материалов
Коррозия контактная — – электрохимическая коррозия, вызванная контактом металлов, имеющих разные стационарные потенциалы в данном электролите. [ГОСТ 5272 68] Рубрика термина: Виды коррозии Рубрики энциклопедии: Абразивное оборудование, Абразивы, Автодороги … Энциклопедия терминов, определений и пояснений строительных материалов
коррозия блуждающим током — Электрохимическая коррозия металла под воздействием блуждающего тока. [ГОСТ 5272 68] Тематики коррозия металлов … Справочник технического переводчика
Книги
- Механика разрушения, Г. П. Черепанов. Книга посвящена механике разрушения широкого класса конструкционных и природных материалов, включая металлы, композиты, горные породы, стекла, полимеры и керамические материалы. Книга состоит… Подробнее Купить за 3559 грн (только Украина)
- Механика разрушения, Черепанов Г.П.. Книга посвящена механике разрушения широкого класса конструкционных и природных материалов, включая металлы, композиты, горные породы, стекла, полимеры и керамические материалы. Книга состоит… Подробнее Купить за 3104 руб
dic.academic.ru
Что такое электрохимическая коррозия. И еще еслив сможете ответить Факторы коррозий (химическая, электрохимическая)
Взаимодействие металла с коррозионной средой (раствором электролита) , при котором ионизация атомов металла и восстановление окислительной компоненты коррозионной среды протекают не в одном акте и их скорости зависят от электродного потенциала.
Электрохимическая коррозия. электрохимическая коррозия является наиболее распространенным типом коррозии металлов. По электрохимическому механизму корродируют металлы в контакте с растворами электролитов (морская вода, растворы кислот, щелочей, солей) . В обычных атмосферных условиях и в земле металлы корродируют также по электрохимическому механизму, т. к. на их поверхности имеются капли влаги с растворенными компонентами воздуха и земли. Электрохимическая коррозия является гетерогенным и многостадийным процессом. Ее причиной является термодинамическая неустойчивость металлов в данной коррозионной среде. Учение о электрохимической коррозии ставит главный вопрос - вопрос о скорости коррозии и тех факторов, которые влияют на нее. С электрохимической точки зрения коррозия металла это не просто процесс окисления металла, т. к. этот переход должен сопровождаться сопряженно идущим восстановительным процессом. В результате ионизации освобождаются электроны и роль второго восстановительного процесса состоит в их ассимиляции подходящим окислителем (Д) , образующим устойчивое соединение Ионизация и процесс ассимиляции электронов каким либо элементом среды (обычно Н ионы или О )представляет собой электрохимический процесс. Факторы: факторы коррозии. Внутренние факторы характеризуют влияние на вид и скорость коррозии природы металла (состав, структура и т. д.) . Внешние факторы определяют влияние состава коррозионной среды и условий протекания коррозии (температура, давление и т. д.) .
touch.otvet.mail.ru











